Mở đầu (trang 26) SGK Hóa 11 Cánh diều Bài 4: Vì sao người ta phải bơm khí nitrogen vào các khoang chứa của tàu chở dầu sau khi chuyển dầu ra khỏi khoang?
- Người ta phải bơm khí nitrogen vào các khoang chứa của tàu chở dầu sau khi chuyển dầu ra khỏi khoang để làm giảm nồng độ của oxygen, giảm nguy cơ cháy nổ. Do tính chất kém hoạt động hoá học (tính trơ), nitrogen không oxi hoá các chất khác ở nhiệt độ thường.
I. Trạng thái tự nhiên của nguyên tố nitrogen
Câu hỏi 1 (trang 26) SGK Hóa 11 Cánh diều Bài 4: Hãy nêu quan điểm của em về phát biểu: “Nitrogen là nguyên tố đặc trưng cho sự sống”.
Trả lời:
“Nitrogen là nguyên tố đặc trưng cho sự sống” vì:
- Nguyên tố nitrogen có trong cơ thể của mọi sinh vật chủ yếu ở dạng các hợp chất hữu cơ như amino acid, nucleic acid, protein, chlorophyll (chất diệp lục),... Các hợp chất này đóng vai trò quan trọng trong những quá trình sinh hoá của sinh vật.
II. Đơn chất nitrogen
Luyện tập 1 (trang 27) SGK Hóa 11 Cánh diều Bài 4: Cho biết năng lượng liên kết của phân tử fluorine, nitrogen lần lượt là 159 kJ mol−1 và 946 kJ mol−1.
a) Giải thích nguyên nhân chính dẫn đến sự khác biệt giá trị năng lượng liên kết giữa hai phân tử trên.
b) Cho biết chất nào hoạt động hoá học hơn.
Lời giải:
a) Sự khác biệt giá trị năng lượng liên kết là liên kết giữa phân tử fluorine là liên kết đơn, còn nitrogen là liên kết ba.
b) Fluorine hoạt động hóa học mạnh hơn, vì năng lượng liên kết của nitrogen > fluorine (946 > 159) nên liên kết phân tử nitrogen khó phá vỡ - hoạt động kém.
Câu hỏi 2 (trang 27) SGK Hóa 11 Cánh diều Bài 4: Dựa vào giá trị biến thiên enthalpy chuẩn của phản ứng, hãy cho biết phản ứng giữa nitrogen với hydrogen hay oxygen diễn ra thuận lợi hơn.
Trả lời:

Luyện tập 2 (trang 27) SGK Hóa 11 Cánh diều Bài 4: Sử dụng kiến thức hoá học để giải thích câu ca dao sau:
“Lúa chiêm lấp ló đầu bờ
Hễ nghe tiếng sấm, phất cờ mà lên”
Lời giải:
Khi có sấm sét, nitrogen và oxygen trong không khí phản ứng với nhau tạo thành nitrogen monoxide (NO):
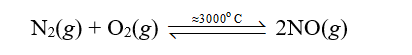
Sau đó, nitrogen monoxide nhanh chóng bị oxi hoá bởi oxygen trong khí quyển tạo thành nitrogen dioxide (NO2):
2NO(g) + O2(g) → 2NO2(g)
Tiếp theo là quá trình nitrogen dioxide chuyển thành acid trong nước mưa, theo phản ứng:
4NO2(g) + 2H2O(l) + O2(g) → 4HNO3(aq)
Nước mưa với nồng độ acid phù hợp sẽ cũng cấp đạm cho đất ở dạng ion nitrate cần thiết cho cây trồng.
Bài tập
Bài tập 1 (trang 29) SGK Hóa 11 Cánh diều Bài 4: Dựa vào các giá trị năng lượng liên kết, hãy dự đoán ở nhiệt độ thường thì đơn chất nitrogen hay chlorine dễ phản ứng với hydrogen hơn. Cho biết năng lượng liên kết Cl − Cl trong phân tử chlorine là 243 kJ.mol-1.
Lời giải:
Năng lượng liên kết trong phân tử nitrogen: Eb(N ≡ N) = 946 kJ.mol-1
Năng lượng liên kết trong phân tử chlorine: Eb(Cl - Cl ) = 243 kJ.mol-1
Vì liên kết đơn trong phân tử chlorine nhỏ, dễ bị phá vỡ hơn so với liên kết ba trong phân tử nitrogen nên phân tử chlorine dễ phản ứng với hydrogen hơn.
Bài tập 2 (trang 29) SGK Hóa 11 Cánh diều Bài 4: Viết phương trình hoá học của phản ứng giữa nitrogen với hydrogen và với oxygen. Nêu ứng dụng của mỗi phản ứng này trong thực tế.
Lời giải:
- Phản ứng của nitrogen với hydrogen:
![]()
Trong thực tế, phản ứng này được ứng dụng trong công nghiệp để sản xuất NH3 – nguyên liệu để sản xuất phân bón, nitric acid …
- Phản ứng của nitrogen với oxygen:
![]()
Trong khí quyển, phản ứng này chính là sự khởi đầu cho quá trình tạo thành ion nitrate, được coi là một nguồn cung cấp đạm tự nhiên cho đất.
Bài tập 3 (trang 29) SGK Hóa 11 Cánh diều Bài 4: Trong công nghiệp, ammonia được sản xuất dựa vào phản ứng thuận nghịch giữa nitrogen và hydrogen trong thiết bị kín.
a) Khi phản ứng đạt trạng thái cân bằng thì trong thiết bị sẽ có các khí nào?
b) Hãy tìm hiểu về nhiệt độ hoá lỏng của mỗi khí có trong thiết bị. Từ đó cho biết, nếu giữ nguyên áp suất và làm lạnh thiết bị thì khí nào sẽ hoá lỏng đầu tiên.
Lời giải:
N2 + 2H2 ⇌ 2NH3
a) Khi phản ứng đạt trạng thái cân bằng thì trong thiết bị sẽ có các khí: N2, H2, NH3
b)

=> Nếu giữ nguyên áp suất và làm lạnh thiết bị thì khí NH3 sẽ hoá lỏng đầu tiên.
