Mở đầu
Câu hỏi SGK Hóa 11 Kết nối tri thức Bài 24 (trang 145): Vị chua của giấm và các loại quả như khế, chanh, táo, me,.... đều được tạo bởi carboxylic acid. Vậy carboxylic acid chứa nhóm chức nào và có các tính chất đặc trưng gì?
Trả lời:
– Carboxylic acid là các hợp chất hữu cơ trong phân tử có nhóm – COOH liên kết với nguyên tử carbon (trong gốc hydrocarbon hoặc – COOH) hoặc nguyên tử hydrogen.
– Tính chất đặc trưng: carboxylic acid thể hiện tính acid và tham gia phản ứng ester hoá.
– Carboxylic acid mạch ngắn là chất lỏng, tan tốt trong nước. Carboxylic acid mạch dài là chất rắn và ít tan trong nước.
I. Khái niệm, danh pháp
1. Khái niệm
* Hoạt động nghiên cứu SGK Hóa 11 Kết nối tri thức Bài 24 (trang 145): Nhiều carboxylic acid tồn tại trong tự nhiên. Hãy nhận xét đặc điểm chung về cấu tạo của các carboxylic acid dưới đây:

Trả lời:
Carboxylic acid là các hợp chất hữu cơ trong phân tử có nhóm –COOH liên kết với nguyên tử carbon (trong gốc hydrocarbon hoặc –COOH) hoặc nguyên tử hydrogen.
2. Danh pháp
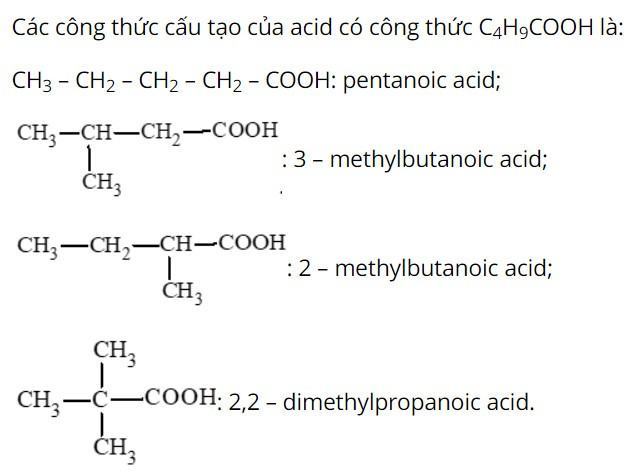
Câu hỏi 1 SGK Hóa 11 Kết nối tri thức Bài 24 (trang 147): Viết các công thức cấu tạo và gọi tên theo danh pháp thay thế của các acid có công thức C4H9COOH.
Trả lời:
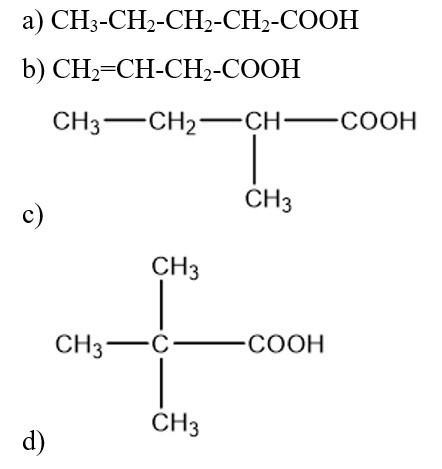
Câu hỏi 2 SGK Hóa 11 Kết nối tri thức Bài 24 (trang 147): Viết công thức cấu tạo của các carboxylic acid có tên gọi dưới đây:
a) pentanoic acid;
b) but-3-enoic acid;
c) 2-methylbutanoic acid;
d) 2,2-dimethylpropanoic acid.
Trả lời:
III. Tính chất vật lí
* Hoạt động nghiên cứu SGK Hóa 11 Kết nối tri thức Bài 24 (trang 147): Tại sao trong các hợp chất hữu cơ có phân tử khối xấp xỉ nhau dưới đây, carboxylic acid có nhiệt độ sôi cao nhất?
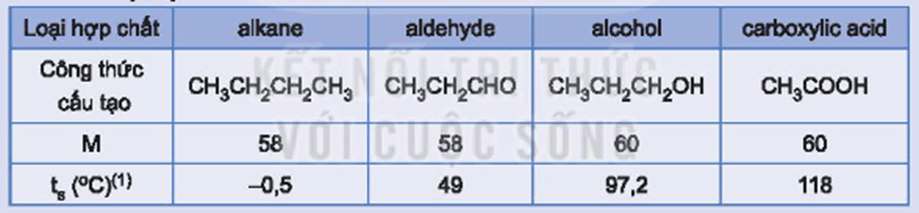
Trả lời:
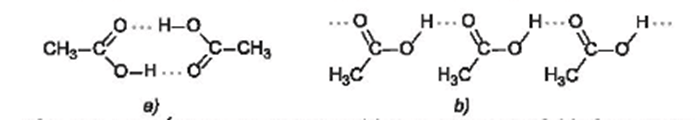
Carboxylic acid có nhiệt độ sôi cao hơn so với hydrocarbon, alcohol, hợp chất carbonyl có phân tử khối tương đương là bởi vì phân tử carboxylic acid chứa nhóm carboxyl phân cực. Các phân tử carboxylic acid liên kết hydrogen với nhau tạo thành dạng dimer hoặc dạng liên phân tử.
Ví dụ:
IV. Tính chất hóa học
1. Tính acid
* Hoạt động nghiên cứu SGK Hóa 11 Kết nối tri thức Bài 24 (trang 148): Trong dung dịch nước, carboxylic acid phân li không hoàn toàn theo cân bằng:

Hằng số cân bằng của phương trình phân li một số carboxylic acid được cho trong Bȧng 24.3.

Hãy nhận xét về khả năng phân li của carboxylic acid. Chúng là các acid mạnh hay yếu và có các phản ứng đặc trưng nào?
Trả lời:
- Trong dung dịch, chỉ một phần nhỏ carboxylic acid phân li thành ion, vì vậy carboxylic acid là những acid yếu. Chúng thể hiện đầy đủ tính chất của acid: tác dụng với kim loại, oxide kim loại, muối, base.
* Hoạt động thí nghiệm SGK Hóa 11 Kết nối tri thức Bài 24 (trang 149): Tính acid của acetic acid
Chuẩn bị: dung dịch acetic acid 10%, dung dịch Na2CO3 10%, bột Mg; ống nghiệm, giấy quỳ.
Tiến hành:
1. Phản ứng với chất chỉ thị:
Nhỏ một giọt dung dịch acetic acid 10% lên mẩu giấy quỳ.
Quan sát và mô tả sự thay đổi màu sắc của giấy quỳ.
2. Phản ứng với kim loại:
- Cho 1 – 2 mL dung dịch acetic acid 10% vào ống nghiệm (1).
- Thêm tiếp một ít bột Mg vào ống nghiệm (1).
Quan sát và mô tả hiện tượng xảy ra trong ống nghiệm (1).
3. Phản ứng với muối:
- Cho 1 – 2 mL dung dịch Na2CO3 10% vào ống nghiệm (2).
- Thêm tiếp 1 – 2 mL dung dịch acetic acid 10% vào ống nghiệm (2).
Thực hiện yêu cầu sau:
Quan sát và mô tả hiện tượng xảy ra trong ống nghiệm (2).
Viết phương trình hoá học của các phản ứng xảy ra trong các thí nghiệm trên và giải thích hiện tượng.
Trả lời:
1. Phản ứng với chất chỉ thị: Quỳ tím chuyển sang màu đỏ.
2. Phản ứng với kim loại:
Hiện tượng: Bột Mg tan dần, có khí không màu thoát ra.
Phương trình hoá học: Mg + 2CH3COOH → (CH3COO)2Mg + H2.
3. Phản ứng với muối:
Hiện tượng: Tạo dung dịch không màu và có khí thoát ra.
Phương trình hoá học: 2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O.
Câu hỏi 4 SGK Hóa 11 Kết nối tri thức Bài 24 (trang 149): Viết phương trình hoá học phản ứng giữa acetic acid với các chất sau:
a) Ca;
b) Cu(OH)2;
c) CaO;
d) K2CO3.
Trả lời:
a) 2CH3COOH + Ca → (CH3COO)2Ca + H2 ↑
b) CH3COOH + Cu(OH)2 → (CH3COO)2Cu + H2O
c) 2CH3COOH + CaO → (CH3COO)2Ca + H2O
d) 2CH3COOH + K2CO3 → 2CH3COOK + CO2 + H2O
Câu hỏi 5 SGK Hóa 11 Kết nối tri thức Bài 24 (trang 149):
a) Khi có cặn màu trắng (thành phần chính là CaCO3) bám ở đáy ấm đun nước, vòi nước, thiết bị vệ sinh,... có thể dùng giấm để loại bỏ các vết cặn này. Hãy giải thích.
b) Các đồ vật bằng đồng sau một thời gian để trong không khí thường bị xỉn màu, dùng khăn tẩm một ít giấm rồi lau các đồ vật này, chúng sáng bóng trở lại. Hãy giải thích.
Trả lời:
a) Khi có cặn màu trắng (thành phần chính là CaCO3) bám ở đáy ấm đun nước, vòi nước, thiết bị vệ sinh,… có thể dùng giấm để loại bỏ các vết cặn này. Nguyên dân là do giấm là dung dịch acetic acid có nồng độ 2 – 5%, do đó giấm có thể tác dụng với CaCO3 (thành phần chính của cặn bám ở đáy ấm đun nước, vòi nước, thiết bị vệ sinh, …) tạo thành muối tan.
PHTT: CaCO3 + 2CH3COOH → (CH3COO)2Ca + CO2 + H2O.
b) Đồ đồng bị xỉn màu do lớp đồng ngoài của đồ đồng đã bị oxi hoá sau một thời gian để trong không khí, sau đó màu đồng xỉn sẽ chuyển sang màu xanh dương dưới sự tác động của CO2 và hơi ẩm.
Cu + H2O + O2 + CO2 → CuCO3.Cu(OH)2
Giấm là dung dịch acetic acid có nồng độ 2 – 5% do đó có thể phản ứng với lớp gỉ đồng này và làm sạch chúng. Do đó, khi dùng khăn tẩm một ít giấm (CH3COOH) rồi lau các đồ vật này, chúng sáng bóng trở lại.
2CH3COOH + CuCO3 → (CH3COO)2Cu + CO2 + H2O
2CH3COOH + Cu(OH)2 → (CH3COO)2Cu + 2H2O
2. Phản ứng ester hóa
* Hoạt động nghiên cứu SGK Hóa 11 Kết nối tri thức Bài 24 (trang 150): Nghiên cứu phản ứng ester hoá – điều chế ethyl acetate
Điều chế ethyl acetate trong phòng thí nghiệm được tiến hành như sau:
- Cho khoảng 2 mL ethanol và 2 mL acetic acid tuyệt đối vào ống nghiệm, lắc đều hỗn hợp.
- Thêm khoảng 1 mL dung dịch H2SO4 đặc, lắc nhẹ để các chất trộn đều với nhau.
- Kẹp ống nghiệm vào kẹp gỗ rồi đặt ống nghiệm vào cốc nước nóng (khoảng 60 °C - 70 °C) trong khoảng 5 phút, thỉnh thoảng lắc đều hỗn hợp. Sau đó lấy ống nghiệm ra khỏi cốc nước nóng, để nguội hỗn hợp rồi rót sang ống nghiệm khác chứa 5 mL dung dịch muối ăn bão hoà.
Thực hiện yêu cầu:
1. Mô tả hiện tượng, viết phương trình hoá học của phản ứng ester hoá xảy ra trong thí nghiệm trên.
2. Vai trò của sulfuric acid trong thí nghiệm trên là gì?
Trả lời:
1. Hiện tượng: Phản ứng sinh ra chất lỏng, nhẹ hơn nước, có mùi thơm đặc trưng.
Phương trình hoá học:
CH3COOH + C2H5OH CH3COOC2H5 + H2O.
2. Sulfuric acid trong thí nghiệm trên vừa là chất xúc tác, vừa có tác dụng hút nước, do đó góp phần làm tăng hiệu suất tạo ester.
Câu hỏi 6 SGK Hóa 11 Kết nối tri thức Bài 24 (trang 151): Methyl butyrate là ester tạo mùi đặc trưng của quả táo, em hãy viết phương trình hoá học của phản ứng điều chế methyl butyrate từ carboxylic acid và alcohol tương ứng.
Trả lời:
- Methylbutyrate là một chất chuyển hóa của axit amin leucine, tổng hợp các protein cơ giúp bảo vệ và tái tạo khối cơ, ngăn protein cơ mất đi. HMB có nhiều trong sữa bột công thức Ensure, các loại thực phẩm khác như thịt bò, trứng, trái bơ, bông cải.
- Methyl butyrate: CH3CH2CH2COOCH3
-Phương trình hóa học: CH3CH2CH2COOH + CH3OH → CH3CH2CH2COOCH3 + H2O
Câu hỏi 7 SGK Hóa 11 Kết nối tri thức Bài 24 (trang 151): Methyl salicylate là hợp chất thuộc loại ester được dùng làm cao dán giảm đau, kháng viêm ngoài da. Methyl salicylate được tổng hợp từ phản ứng ester hoá giữa salicylic acid và methanol. Hãy hoàn thành phương trình hoá học của phản ứng tổng hợp methyl salicylate:
Trả lời:
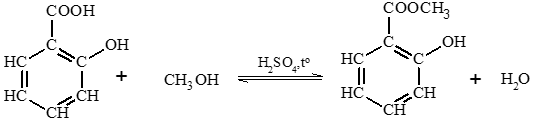
VI. Ứng dụng
* Hoạt động nghiên cứu SGK Hóa 11 Kết nối tri thức Bài 24 (trang 151): Em hãy tìm hiểu và trình bày ứng dụng của một carboxylic acid.
Trả lời:
– Sản xuất vinyl acetate và cellulose acetate.
– Tổng hợp aluminium monoacetate (Al(OH)2COOCH3) làm chất cầm màu trong công nghiệp dệt may, tổng hợp ethyl acetate, butyl acetate làm dung môi (để pha sơn).
– Vinyl acetate được dùng sản xuất keo dán và chất kết dính trong sản xuất giấy, sản xuất tơ (tơ vinylon),…
– Rất nhiều carboxylic acid khác được ứng dụng trong đời sống và sản xuất. Acrylic acid và methacrylic acid được dùng để sản xuất thuỷ tinh hữu cơ.
– Acetic acid còn được sử dụng để tổng hợp aluminium monoacetate (Al(OH)2COOCH3) làm chất cầm màu trong công nghệ dệt may.
– Dung dịch acetic acid 2 – 5% được dùng làm giấm ăn, làm chất tẩy cặn trong siêu đun nước và nhiều ứng dụng trong đời sống hàng ngày.
